近日,昆明理工大学季维智/牛昱宇团队联合美国北卡罗来纳大学研究团队在Brain发表了题为“α-Synuclein aggregation and brain atrophy in SNCA-A53T transgenic monkeys correlate with parkinsonism”的研究。帕金森病(Parkinson’ Disease, PD)是一种常见的神经退行性疾病。随着中国人口老龄化的加剧,近三十年间,我国与帕金森病相关的疾病负担指标均呈快速上升趋势,严重影响老年人群的健康。PD通常以隐匿的睡眠障碍和躯体症状开始,当静止性震颤、运动迟缓等典型运动症状出现时,中脑黑质的多巴胺能神经元已发生大量丢失,此时治疗效果有限。因此,阐明PD前驱期的病理生理变化,是实现早期诊断与疾病干预的关键。然而,现有临床前模型,尤其是广泛使用的小鼠模型,在模拟人类PD复杂的、渐进的多系统病理及非运动症状(如与人类高度相似的快速眼动睡眠行为障碍)方面存在局限,极大地制约了对疾病起源和早期干预靶点的探索。

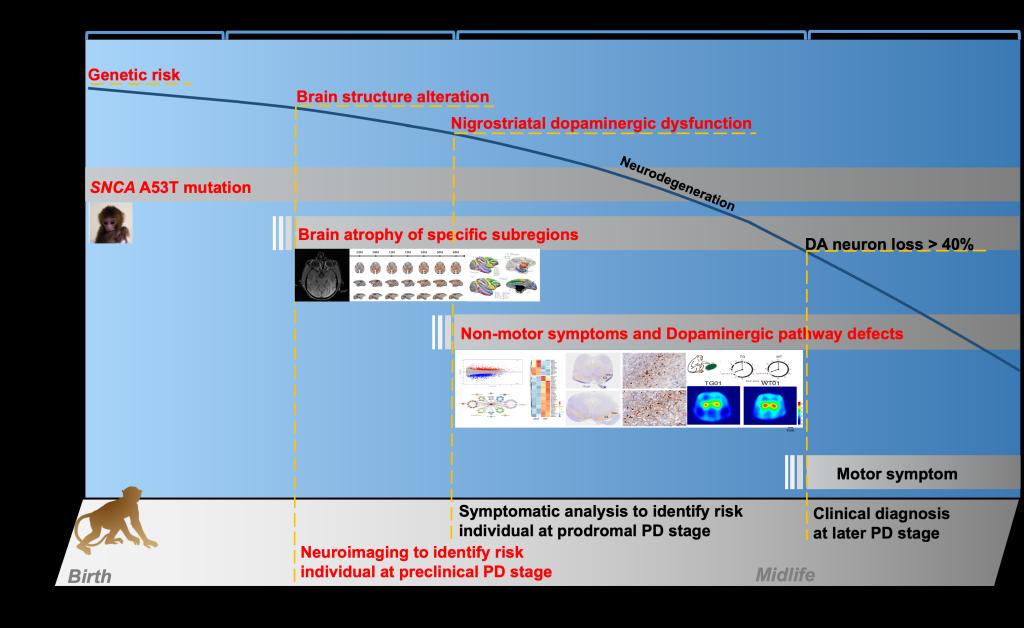
研究者利用SNCA-A53T转基因猕猴模型,从动物出生开始进行长达四年的纵向、多维度系统追踪,成功再现了α-突触核蛋白的进行性病理沉积、不对称性多巴胺能系统损伤、快速眼动睡眠行为障碍、隐匿性的运动与认知缺陷,以及与症状相关的广泛性脑萎缩。研究利用转基因猕猴模型首次系统重现了PD从前驱期到早期的完整病理演进链条,包括分子病理、神经退行、脑网络改变及复杂的临床前驱表型,为在体研究疾病起始机制提供了不可替代的平台。研究明确了睡眠障碍与特定模式的脑结构MRI变化可作为有前景的早期生物标志物组合。同时,研究揭示了星形胶质细胞丢失是早期脑结构改变的关键因素,为开发针对神经胶质细胞的疾病修饰疗法提供了新靶点。
昆明理工大学季维智、牛昱宇、赵璐以及美国北卡罗来纳大学李刚为本研究共同通讯作者。昆明理工大学魏景宽、李树林,以及美国北卡罗来纳大学香槟山分校Dingna Duan和云南省第一人民医院吴昆华为该研究的共同第一作者。该研究得到国家重点研发计划、国家自然科学基金和云南省基础研究计划的支持。
文章链接:https://doi.org/10.1093/brain/awag046
(供稿:灵长类转化医学研究院)
 滇公网安备53011402000430号 All Rights Reserved © Kunming University of Science and Technology
滇公网安备53011402000430号 All Rights Reserved © Kunming University of Science and Technology